A. pengertian asam basa

Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah basa (alkali) berasal dari bahasa Arab yang berarti abu. Basa digunakan dalam pembuatan sabun. Juga sudah lama diketahui bahwa asam dan basa saling menetralkan. Di alam, asam ditemukan dalam buah-buahan, misalnya asam sitrat dalam buah jeruk berfungsi untuk memberi rasa limun yang tajam. Cuka mengandung asam asetat, dan asam tanak dari kulit pohon digunakan untuk menyamak kulit. Asam mineral yang lebih kuat telah dibuat sejak abad pertengahan, salah satunya adalah aqua forti (asam nitrat) yang digunakan oleh para peneliti untuk memisahkan emas dan perak.

Pada tahun 1884, Svante Arrhenius (1859-1897) seorang ilmuwan Swedia yang memenangkan hadiah nobel atas karyanya di bidang ionisasi, memperkenalkan pemikiran tentang senyawa yang terpisah atau terurai menjadi bagian ion-ion dalam larutan. Dia menjelaskan bagaimana kekuatan asam dalam larutan aqua (air) tergantung pada konsentrai ion-ion hidrogen di dalamnya.
Menurut Arrhenius, asam adalah zat yang dalam air melepakan ion H+, sedangkan basa adalah zat yang dalam air melepaskan ion OH–. Jadi pembawa sifat asam adalah ion H+, sedangkan pembawa sifat basa adalah ion OH–. Asam Arrhenius dirumuskan sebagai HxZ, yang dalam air mengalami ionisasi sebagai berikut.
HxZ ⎯⎯→ x H+ + Zx–
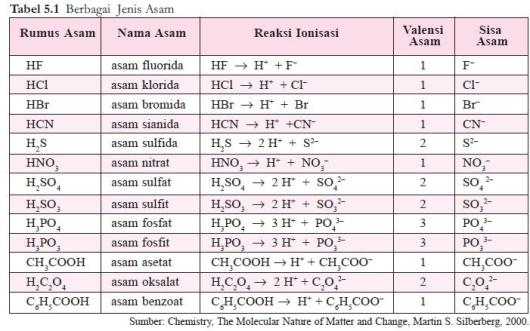
Jumlah ion H+ yang dapat dihasilkan oleh 1 molekul asam disebut valensi asam, sedangkan ion negatif yang terbentuk dari asam setelah melepaskan ion H+ disebut ion sisa asam. Beberapa contoh asam dapat dilihat pada tabel 5.1.
 Basa Arrhenius adalah hidroksida logam, M(OH)x, yang dalam air terurai sebagai berikut.
Basa Arrhenius adalah hidroksida logam, M(OH)x, yang dalam air terurai sebagai berikut.M(OH)x ⎯⎯→ Mx+ + x OH–
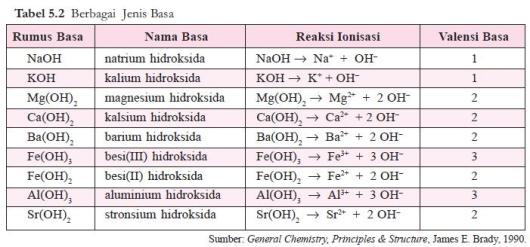
Jumlah ion OH– yang dapat dilepaskan oleh satu molekul basa disebut valensi basa. Beberapa contoh basa diberikan pada tabel 5.2.
Asam sulfat dan magnesium hidroksida dalam air mengion sebagai berikut.
H2SO4 ⎯⎯→ 2 H+ + SO42–
Mg(OH)2 ⎯⎯→ Mg+ + 2 OH–
H2O(l) ←⎯⎯⎯⎯→ H+(aq) + OH–(aq)
- Harga tetapan air adalah:

- Konsentrasi H2O yang terionisasi menjadi H+ dan OH– sangat kecil dibandingkan dengan konsentrasi H2O mula-mula, sehingga konsentrasi H2O dapat dianggap tetap, maka harga K[H2O] juga tetap, yang disebut tetapan kesetimbangan air atau ditulis Kw.
- Jadi,
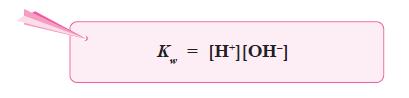
- Pada suhu 25 °C, Kw yang didapat dari percobaan adalah 1,0 × 10–14.
- Harga Kw ini tergantung pada suhu, tetapi untuk percobaan yang suhunya tidak terlalu menyimpang jauh dari 25 °C, harga Kw itu dapat dianggap tetap.
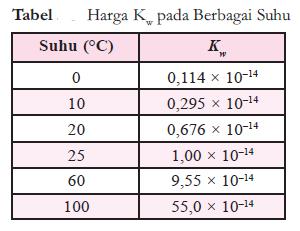
- Harga Kw pada berbagai suhu dapat dilihat pada tabel berikut.


Tidak ada komentar:
Posting Komentar